La inteligencia artificial de Google logra un hito frente a uno de los mayores retos de la biolog¿¬a
Un algoritmo que predice la forma de las prote¿¬nas a partir de su ADN acelerar¿ó la investigaci¿«n de enfermedades como alzh¿Ğimer o diabetes

DeepMind, el laboratorio londinense de inteligencia artificial que Google compr¿« en 2014, ya ha creado programas que ganan siempre al ajedrez, al shogi y al Go, los juegos de tablero m¿ós complejos. Pero el objetivo final de la empresa no est¿ó en los pasatiempos, sino en resolver acuciantes problemas cient¿¬ficos. Su algoritmo AlphaFold, presentado a principios de diciembre en Canc¿▓n, M¿Ğxico, ha ganado una competici¿«n mundial en predecir la estructura tridimensional de prote¿¬nas.
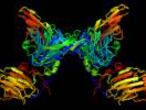
Las prote¿¬nas son las m¿óquinas moleculares de los seres vivos. Cada una es una cadena larga de unidades llamadas amino¿ócidos, como abalorios ensartados en un alambre, que se pliega espont¿óneamente para adoptar una forma compleja y precisa. La estructura final de cada prote¿¬na determina su funci¿«n. Los anticuerpos, por ejemplo, son como ganchos que se acoplan a los microbios. La hemoglobina tiene un hueco que atrapa mol¿Ğculas de ox¿¬geno. El col¿ógeno es parecido a un cable trenzado.
Predecir la estructura de cualquier prote¿¬na a partir de su secuencia de amino¿ócidos se considera uno de los santos griales de la biolog¿¬a. No es tarea menor; los amino¿ócidos son 20 mol¿Ğculas con propiedades qu¿¬micas ligeramente distintas, con lo cual est¿ón unidos por enlaces de diferentes longitudes y ¿óngulos. Se tardar¿¬a m¿ós que la edad del universo en doblar una prote¿¬na por todas sus configuraciones posibles antes de dar con la estructura tridimensional correcta por azar.
Pese a lo esot¿Ğrico de este campo cient¿¬fico, es dif¿¬cil exagerar su importancia. Ciertas enfermedades, como el alzh¿Ğimer, el p¿órkinson, la diabetes o la fibrosis qu¿¬stica, se deben a la acumulaci¿«n de prote¿¬nas mal plegadas, algo que se podr¿¬a evitar conocida la relaci¿«n entre su secuencia y su estructura. Casi todos los medicamentos act¿▓an por acoplamiento a la regi¿«n espec¿¬fica de una prote¿¬na, un proceso que de nuevo depende de la estructura precisa de la diana. Adem¿ós, con la capacidad de predecir exactamente c¿«mo se doblar¿ó una cadena de amino¿ócidos, los cient¿¬ficos pueden dise?ar prote¿¬nas artificiales, por ejemplo para degradar pl¿ósticos o compuestos contaminantes, del organismo o del medio ambiente.
En un comunicado, el equipo de DeepMind ha llamado a este logro su í░primer hito significativoí▒ en la aplicaci¿«n de la inteligencia artificial al progreso cient¿¬fico. í░El problema del pliegue de las prote¿¬nas no est¿ó resuelto todav¿¬aí▒ advierte Paul Bates, un experto en este campo del Instituto Francis Crick, en Reino Unido, que acudi¿« a la presentaci¿«n de AlphaFold en Canc¿▓n. í░El programa de DeepMind acierta m¿ós veces y con m¿ós precisi¿«n que los dem¿ós, pero no resuelve todas las estructurasí▒, explica Bates a Materia. Esto es porque la inteligencia artificial aprende de una base de datos de prote¿¬nas conocidas, y por tanto tropieza con estructuras completamente nuevas.
El concurso que ha ganado AlphaFold, llamado Evaluaci¿«n Cr¿¬tica de Predicci¿«n de Estructuras (CASP en ingl¿Ğs), se celebra cada dos a?os. En ¿Ğl, cada equipo recibe en intervalos de varios d¿¬as nuevas secuencias gen¿Ğticas. Estas se corresponden a prote¿¬nas bien estudiadas en el laboratorio, pero cuya estructura no se ha dado a conocer al p¿▓blico. Los concursantes deben aproximarse lo m¿óximo posible con sus modelos de predicci¿«n a la forma real de la mol¿Ğcula.
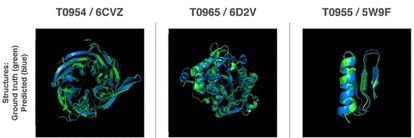
El equipo de Google, que se presentaba por primera vez al certamen, qued¿« primero de 98 concursantes, al estimar con mayor precisi¿«n la estructura de 25 de las 43 prote¿¬nas, seg¿▓n informa The Guardian. Para cada secuencia de amino¿ócidos, suele existir un pliegue correcto, que se corresponde a la configuraci¿«n de mayor estabilidad bioqu¿¬mica. En un laboratorio, se puede observar la forma real de las biomol¿Ğculas mediante t¿Ğcnicas como la resonancia magn¿Ğtica o la cristalograf¿¬a de rayos X, un m¿Ğtodo parecido al que permiti¿« a Rosalind Franklin ver por primera vez la estructura de la doble h¿Ğlice del ADN.
La inteligencia artificial constituye un avance incre¿¬ble con respecto a esas t¿Ğcnicas complejas y costosas, aunque todav¿¬a no es capaz de sustituirlas por completo. DeepMind entren¿« a una red neuronal relacionando la forma y la secuencia g¿Ğnica de miles de prote¿¬nas conocidas. Armado con ese conocimiento, el programa AlphaFold predice la distancia y el ¿óngulo entre cada pareja de amino¿ócidos de la cadena, y luego hace peque?os ajustes a la estructura completa para encontrar la configuraci¿«n m¿ós estable.
Proteins are essential to all known forms of life. Working out how they fold into 3D structures is one of the major outstanding questions in biology and could impact disease understanding, drug discovery, and protein design (2/5) pic.twitter.com/dqe7wdwuJA
— DeepMind (@DeepMind) December 3, 2018
Las aplicaciones m¿Ğdicas m¿ós inmediatas de esta tecnolog¿¬a se ver¿ón en el dise?o de f¿órmacos, incluidos los medicamentos contra el c¿óncer, opina Bates. í░Todav¿¬a no se han conseguido modelos con suficiente precisi¿«n para estoí▒, dice. En un futuro algo m¿ós lejano, podr¿¬a llegar la modificaci¿«n de prote¿¬nas asociadas a enfermedades degenerativas como el alzh¿Ğimer. í░Ya se puede empezar a pensar en esos problemas m¿ós dif¿¬ciles. Esto da un punto de partida".
Los concursantes de DeepMind concluyen que í░queda mucho trabajo por hacer antes de poder tener un impacto cuantificable en el tratamiento de enfermedades, la gesti¿«n del medio ambiente y otras aplicacionesí▒, pero a?aden que í░el potencial es enormeí▒. Seg¿▓n Bates, el algoritmo ideal probar¿¬a cada enlace de la cadena proteica sin necesidad de una referencia externa, pero eso requiere un conocimiento profundo de f¿¬sica inalcanzable todav¿¬a. A pesar de que el equipo de DeepMind llega nuevo a una disciplina bien trillada, í░lo ha hecho mejor que cualquieraí▒, asegura el cient¿¬fico brit¿ónico.
Tu suscripci¿«n se est¿ó usando en otro dispositivo
?Quieres a?adir otro usuario a tu suscripci¿«n?
Si contin¿▓as leyendo en este dispositivo, no se podr¿ó leer en el otro.
FlechaTu suscripci¿«n se est¿ó usando en otro dispositivo y solo puedes acceder a EL PA?S desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripci¿«n a la modalidad Premium, as¿¬ podr¿ós a?adir otro usuario. Cada uno acceder¿ó con su propia cuenta de email, lo que os permitir¿ó personalizar vuestra experiencia en EL PA?S.
En el caso de no saber qui¿Ğn est¿ó usando tu cuenta, te recomendamos cambiar tu contrase?a aqu¿¬.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrar¿ó en tu dispositivo y en el de la otra persona que est¿ó usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aqu¿¬ los t¿Ğrminos y condiciones de la suscripci¿«n digital.