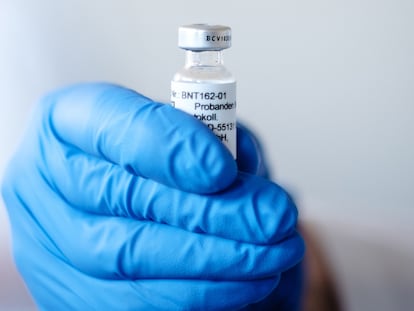
กฐAutorizar la vacuna de emergencia es correr un riesgo que no parece justificadoกฑ
กฐEn una situaciจฎn en la que no parece que vayamos a peor, en adelantar en una semana o dos la vacunaciจฎn tendrจชa que haber un beneficio potencial muy grandeกฑ, dice Cจฆsar Hernจขndez, jefe del Departamento de Medicamentos de Uso Humano de la Aemps


La autorizaciจฎn que ha concedido el Reino Unido a la primera vacuna contra la covid-19 no es tan completa como la que dentro de menos de un mes darจข la Agencia Europea del Medicamento, explica Cจฆsar Hernจขndez (Madrid, 1963), jefe del Departamento de Medicamentos de Uso Humano de la Agencia Espa?ola de Medicamentos y Productos Sanitarios (Aemps). El experto explica en quจฆ se diferencian ambos trจขmites y cree que no merece la pena acelerar la autorizaciจฎn europea, prevista para finales de diciembre.
Pregunta. ?Por quจฆ ha sido mจขs rจขpida la agencia britจขnica que la europea, la EMA?
Respuesta. Porque autoriza una cosa distinta, una especie de uso compasivo, con unos requerimientos distintos de una autorizaciจฎn completa, que es lo que plantean el resto de paจชses europeos. La britจขnica y la que parece que darจข la FDA [la agencia estadounidense] son autorizaciones de uso de emergencia, no de comercializaciจฎn, con unos requisitos mจขs bajos. Es como un uso compasivo, pero colectivo, como lo que hicieron inicialmente con la hidroxicloroquina o el remdesivir.
P. En la prจขctica, ?cuจขl es la diferencia? ?La autorizaciจฎn permite vacunar a todo el mundo?
R. La autorizaciจฎn irจข dirigida a unos grupos especจชficamente, pero lo mจขs diferente es el soporte de calidad del producto. La agencia inglesa ha anunciado que va a ir autorizando lote a lote, es decir, tendrจข que ir dando mจขs autorizaciones, mientras que una autorizaciจฎn completa กชpor eso lleva mจขs tiempoกช permite seguir el flujo habitual del resto de vacunas y medicamentos.
P. ?Influye esto en la calidad?
R. Una de las cosas mจขs importantes de las vacunas y de los medicamentos biolจฎgicos es asegurar que los lotes son iguales, que cuando los fabricas siempre tengan, por ejemplo, la misma cantidad de antจชgeno. Y en estas molจฆculas que son tan complejas, donde es tan fจขcil que el ARN mensajero se degrade, peque?as variaciones podrจชan dar lugar a cambios en los efectos.
P. ?Quจฆ otras diferencias hay?
R. En el uso de emergencia todavจชa no tienes todos los datos del medicamento, pero los tienes parciales y como estจขs en una situaciจฎn grave, en este caso en una pandemia, aจฒn faltando datos merece la pena autorizar. La legislaciจฎn que lo permite es comจฒn al resto de paจชses europeos. Otra diferencia es que con una autorizaciจฎn de comercializaciจฎn la responsabilidad sobre el producto recae en la compa?จชa, mientras que con un uso compasivo estas quedan exentas porque no es un medicamento autorizad, sino uno del que se permite la distribuciจฎn por la situaciจฎn de pandemia y analizando el riesgo-beneficio.
P. ?Podrจชan otros paจชses europeos dar autorizaciจฎn de emergencia?
R. No creo que lo hagan porque eso romperจชa la armonizaciจฎn y el consenso actuales.
P. ?Por quจฆ prefiere la EMA respetar sus plazos?
R. En una situaciจฎn en la que epidemiolจฎgicamente no parece que vayamos a peor, para adelantar en una semana o dos la vacunaciจฎn tendrจชa que haber un beneficio potencial muy grande para el riesgo que se corre. Todas las decisiones de medicamentos se basan en esa relaciจฎn. Un riesgo muy grande se puede aceptar si vas a tener un beneficio que lo supera. Del mismo modo, con un beneficio muy peque?o y un riesgo nulo tambiจฆn lo puedes asumir, pero con un beneficio incierto, y con dos semanas para una autorizaciจฎn completa, correr ese riesgo no parece muy justificado. Y una autorizaciจฎn concedida por la misma vจชa que el resto de medicamentos contribuye a generar mจขs confianza en la gente.
Informaciจฎn sobre el coronavirus
- Aquจช puede seguir la จฒltima hora sobre la evoluciจฎn de la pandemia
- Buscador de restricciones: ?Quจฆ puedo hacer en mi municipio?
- Asจช evoluciona la curva del coronavirus en el mundo
Tu suscripciจฎn se estจข usando en otro dispositivo
?Quieres a?adir otro usuario a tu suscripciจฎn?
Si continจฒas leyendo en este dispositivo, no se podrจข leer en el otro.
FlechaTu suscripciจฎn se estจข usando en otro dispositivo y solo puedes acceder a EL PA?S desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripciจฎn a la modalidad Premium, asจช podrจขs a?adir otro usuario. Cada uno accederจข con su propia cuenta de email, lo que os permitirจข personalizar vuestra experiencia en EL PA?S.
?Tienes una suscripciจฎn de empresa? Accede aquจช para contratar mจขs cuentas.
En el caso de no saber quiจฆn estจข usando tu cuenta, te recomendamos cambiar tu contrase?a aquจช.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrarจข en tu dispositivo y en el de la otra persona que estจข usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquจช los tจฆrminos y condiciones de la suscripciจฎn digital.
Sobre la firma