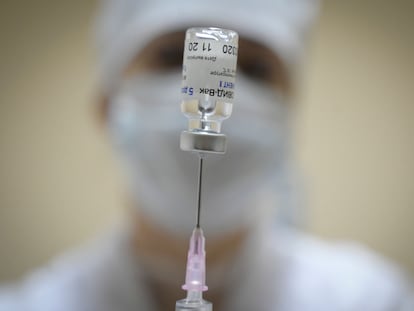
La EMA encuentra ¡°posibles v¨ªnculos¡± entre casos muy raros de trombos y la vacuna de AstraZeneca
La agencia se reafirma en la ¡°alta eficacia¡± de la vacuna para evitar la enfermedad e insiste en que los beneficios siguen siendo muy superiores a los riesgos

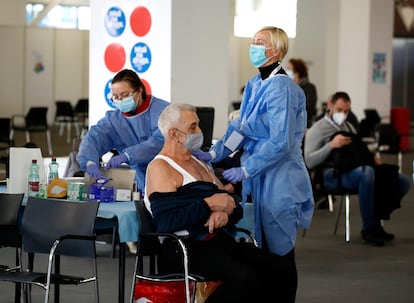
La Agencia Europea del Medicamento (EMA, por sus siglas en ingl¨¦s) ha concluido este mi¨¦rcoles que los co¨¢gulos de sangre deben ser incorporados como ¡°efectos secundarios muy raros¡± de la vacuna de AstraZeneca. As¨ª lo ha considerado el Comit¨¦ de Evaluaci¨®n de Riesgos de Farmacovigilancia (PRAC), reunido desde este martes para evaluar 86 casos de trombosis que le han trasladado hasta ahora las autoridades nacionales europeas, la mayor¨ªa en mujeres menores de 60 a?os. La EMA, que no ha confirmado factores de riesgo por edad ni g¨¦nero, sigue considerando que los beneficios contin¨²an siendo superiores a los riesgos. ¡°La vacuna es altamente efectiva para salvar vidas y la vacunaci¨®n es extremadamente importante¡±, ha afirmado la directora ejecutiva de la EMA, Emer Cooke. Tras la elaboraci¨®n del informe, son los pa¨ªses quienes deben decidir a qui¨¦n administran la vacuna. Los 27 ministros de Sanidad se re¨²nen por videoconferencia desde las 18.00 para acordar las medidas que deben derivarse de ese dictamen.
El informe es el resultado de una investigaci¨®n en profundidad de 86 casos de trombos reportados por las autoridades nacionales hasta el 22 de marzo, de las cuales 18 acabaron en fallecimiento. De estos, 62 trombos eran cerebrales y 24 abdominales. Con posterioridad a esa fecha, los pa¨ªses siguieron llevando casos a la EMA, de modo que hasta el 4 de abril pasado se hab¨ªan registrado 222 casos en toda la UE. Hasta ese d¨ªa, 34 millones de personas hab¨ªan sido vacunadas en los pa¨ªses del Espacio Econ¨®mico Europeo y el Reino Unido.
¡°El riesgo de mortalidad por la covid-19 es mucho mayor que la mortalidad por estos efectos secundarios muy raros¡±, ha sostenido Cooke en una rueda de prensa desde ?msterdam. El mensaje desde la EMA es claro: hay un v¨ªnculo entre los trombos detectados y la administraci¨®n de la vacuna de la farmac¨¦utica anglosueca, pero se trata de casos muy raros y los beneficios de la vacuna siguen primando. ¡°La covid-19 es una enfermedad muy grave, y la vacuna es efectiva evitando la enfermedad, la hospitalizaci¨®n y la mortalidad. En su conjunto, el beneficio es superior al riesgo¡±, ha afirmado Sabine Straus, jefa del comit¨¦ de Seguridad de la EMA. La decisi¨®n se ha tomado tras haber estudiado tambi¨¦n los informes de expertos independientes.
La EMA ha explicado que por ahora no hay un tratamiento espec¨ªfico para esos efectos secundarios. Los pa¨ªses deber¨¢n decidir c¨®mo aplican las conclusiones de ese informe, en especial despu¨¦s de la alarma que se han podido generar por los traspi¨¦s de comunicaci¨®n de los pa¨ªses y de la propia EMA. Los Pa¨ªses Bajos y Alemania hasta ahora hab¨ªan decidido emplear esa vacuna solo con mayores de 60 a?os. Seg¨²n la agencia comunitaria, la mayor¨ªa de los casos que han analizado corresponden a mujeres menores de 60 a?os, que han sufrido un co¨¢gulo en las dos semanas posteriores a haber sido vacunadas. Sin embargo, los expertos comunitarios consideran que de esa circunstancia no pueden extraerse conclusiones generales. De hecho, Straus ha explicado que dado que hay diferencias importantes entre pa¨ªses en c¨®mo se est¨¢ usando la vacuna, con una mayor administraci¨®n a mujeres de menos edad, no se puede concluir que ese grupo de poblaci¨®n tenga un riesgo mayor.
La agencia europea empez¨® a investigar casos de trombos entre ciudadanos que recibieron la vacuna ¡ªmuy infrecuentes¡ª, que a mitad del mes pasado supusieron un par¨®n en la inmunizaci¨®n con ese f¨¢rmaco en 16 pa¨ªses de la Uni¨®n Europea, entre ellos Espa?a. En sus primeras evaluaciones, la EMA ya concluy¨® que la vacuna era ¡°segura y efectiva¡± y destac¨® que los beneficios que aportaba a la sociedad superaban con creces a los riesgos. El medicamento ha demostrado una eficacia del 100% en casos graves de covid-19 y, a diferencia de las vacunas de Pfizer-BioNTech y Moderna, puede conservarse en frigor¨ªficos normales.
Esa primera evaluaci¨®n permiti¨® que la mayor¨ªa de los socios comunitarios reactivaran sus procesos de vacunaci¨®n con AstraZeneca, entre ellos Espa?a. La EMA, no obstante, no descart¨® el v¨ªnculo con episodios tromboemb¨®licos, pero advirti¨® de que necesitaba una mayor investigaci¨®n. Ante los casos detectados por las autoridades sanitarias, los Pa¨ªses Bajos y Alemania decidieron utilizar el f¨¢rmaco solo en personas mayores de 60 a?os. En Espa?a, se ampli¨® su uso, inicialmente solo aprobado hasta los 55 a?os, a los menores de 65 a?os. La presidencia de la UE, que este semestre ocupa Portugal, ha convocado un consejo de ministros de Sanidad para esta tarde con el objetivo de adoptar una decisi¨®n conjunta para los 27 pa¨ªses de la UE.
La EMA ha estado investigando 86 casos de esos extra?os trombos, de los cuales 62 son cerebrales y 24 abdominales. De estos, 18 resultaron fallecidos, seg¨²n un comunicado distribuido por la agencia europea. Desde la EMA se ha venido insistiendo en que se trata de episodios raros, puesto que ya se han administrado m¨¢s de nueve millones de inyecciones en la UE. Sin embargo, las declaraciones de dos directivos de la agencia en medios italianos esta semana sobre esa relaci¨®n de la vacuna con los trombos ha generado todav¨ªa m¨¢s confusi¨®n, de modo que incluso regiones como Castilla y Le¨®n decidieron volver a suspender de forma cautelar, pese a suscitar malestar en el Gobierno central, su empleo hasta conocer el dictamen de la agencia europea.
El jefe de estrategia de vacunaci¨®n de EMA, Marco Cavalieri, afirm¨® en el diario italiano Il Messagero que, a su juicio, los v¨ªnculos entre la vacuna y los casos de coagulaci¨®n sangu¨ªnea eran ¡°claros¡±. ¡°En mi opini¨®n, podemos decirlo, hay claramente una asociaci¨®n con la vacuna. Sin embargo, todav¨ªa no sabemos qu¨¦ causa esta reacci¨®n. Estas trombosis cerebrales con d¨¦ficit de plaquetas parecen ser el principal evento para investigar. En resumen: en las pr¨®ximas horas diremos que hay una conexi¨®n, pero todav¨ªa tenemos que entender c¨®mo ocurre¡±, afirm¨®. En otra entrevista distinta en La Stampa, Armando Genazzani, otro directivo de la EMA, afirm¨® que ese v¨ªnculo era ¡°plausible¡±.
Las declaraciones de ambos directivos se produc¨ªan justo el d¨ªa en el que el Comit¨¦ de Evaluaci¨®n de Riesgos de Farmacovigilancia de la EMA se reun¨ªa para proporcionar una ¡°recomendaci¨®n actualizada¡± tras haber analizado todos los episodios raros de trombosis y haber estudiado los trabajos desarrollados por expertos independientes. Es decir, ambos directivos vinieron a avanzar las conclusiones de una reuni¨®n que dura toda la semana. El organismo advirti¨® de que todav¨ªa no se hab¨ªa adoptado una decisi¨®n, pero tuvo que fijar para este mi¨¦rcoles por la tarde una comparecencia para explicar los resultados de los an¨¢lisis.
La vacuna de AstraZeneca fue la tercera en recibir la autorizaci¨®n de la EMA y la Comisi¨®n Europea para salir al mercado. Antes lo hab¨ªan hecho las de Pfizer-BioNTech y Moderna, y despu¨¦s la de Janssen. La andadura del f¨¢rmaco en la UE ha estado plagada de controversias, contratiempos y encontronazos, despu¨¦s de que la firma anglo-sueca haya ido rebajando sus previsiones de entregas continuamente y haya desbaratado el calendario de vacunaci¨®n del primer trimestre. Para rematarlo, el medicamento ha sido cuestionado por los trombos o por la falta de datos sobre su eficacia en mayores de 65 a?os. La EMA, sin embargo, ha ido despejando esas dudas: en plena tercera oleada de contagios en la UE, esa vacuna ha resultado eficaz para rebajar contagios, ingresos y muertes.
El Reino Unido desaconseja el f¨¢rmaco para menores de 30
Wei Shen Lim, presidente del Comit¨¦ de Vacunaci¨®n, ha sostenido en una rueda de prensa que era preferible que este grupo de edad se vacunara con las otras dos inmunizaciones aprobadas en el pa¨ªs, la de Pfizer y BioNTech y la de Moderna. Quienes lo deseen podr¨¢n seguir vacun¨¢ndose con las dosis anglosuecas.
El experto del JCVI ha subrayado que el anuncio iba dirigido solo a la gente joven, con menor riesgo de hospitalizaci¨®n por covid, y que se realizaba por una cuesti¨®n de ¡°precauci¨®n¡±, y no porque el comit¨¦ tenga dudas sobre la seguridad de la vacuna. El medicamento, desarrollado junto a la Universidad de Oxford, es el m¨¢s extendido en el pa¨ªs y su eficacia siempre ha sido defendida por el Gobierno brit¨¢nico. Fue as¨ª incluso cuando varios pa¨ªses europeos decidieron suspender su uso a mediados del mes pasado tras detectarse algunos casos de trombosis en vacunados con el f¨¢rmaco, que se ha suministrado a decenas de millones de personas en Europa. ¡°Como han afirmado los ¨®rganos reguladores, esta vacuna es segura, efectiva y ha salvado ya miles de vidas. La gran mayor¨ªa de la poblaci¨®n deber¨ªa seguir poni¨¦ndosela cuando se la ofrezcan¡±, ha dicho este mi¨¦rcoles el primer ministro brit¨¢nico, Boris Johnson.
La consejera delegada de la Agencia Reguladora de Medicinas y Productos Sanitarios del Reino Unido, June Raine, ha indicado que hasta el 31 de marzo se han registrado 79 casos de trombos con un bajo n¨²mero de plaquetas en personas que recibieron la primera dosis de AstraZeneca. De ellos, 19 personas han muerto, tres de ellas menores de 30 a?os ¡ªaunque en algunos casos se desconoce la causa¡ª. Del total de afectados, de entre 18 y 79 a?os, 51 son mujeres y 28 hombres, indic¨® Raine. El Reino Unido ha inyectado m¨¢s de 18 millones de dosis de la vacuna de AstraZeneca. Los organismos reguladores siguen recomendando el f¨¢rmaco en adultos de mayores de 30 a?os al considerar que ¡°los beneficios sobradamente compensan los riegos¡±, en palabras de Raine.
La Agencia Reguladora ha aclarado que los j¨®venes de grupos prioritarios, como el sector sanitario o personas con un sistema inmune debilitado, que hayan recibido una primera dosis de la vacuna de AstraZeneca deben recibir la segunda conforme al calendario previsto.
Tu suscripci¨®n se est¨¢ usando en otro dispositivo
?Quieres a?adir otro usuario a tu suscripci¨®n?
Si contin¨²as leyendo en este dispositivo, no se podr¨¢ leer en el otro.
FlechaTu suscripci¨®n se est¨¢ usando en otro dispositivo y solo puedes acceder a EL PA?S desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripci¨®n a la modalidad Premium, as¨ª podr¨¢s a?adir otro usuario. Cada uno acceder¨¢ con su propia cuenta de email, lo que os permitir¨¢ personalizar vuestra experiencia en EL PA?S.
?Tienes una suscripci¨®n de empresa? Accede aqu¨ª para contratar m¨¢s cuentas.
En el caso de no saber qui¨¦n est¨¢ usando tu cuenta, te recomendamos cambiar tu contrase?a aqu¨ª.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrar¨¢ en tu dispositivo y en el de la otra persona que est¨¢ usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aqu¨ª los t¨¦rminos y condiciones de la suscripci¨®n digital.
Sobre la firma