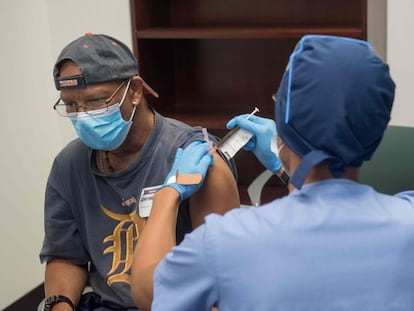
Pfizer anuncia un 95% de eficacia de su vacuna y solicitaršą su aprobacišźn de emergencia
La inyeccišźn, desarrollada en colaboracišźn con BioNTech, es la primera en demostrar plena validez estadšȘstica
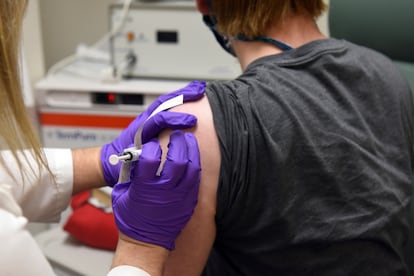
La farmacšŠutica estadounidense Pfizer acaba de anunciar que su vacuna tiene un 95% de eficacia. Los nuevos datos tienen por primera vez plena validez estadšȘstica, pues el ensayo clšȘnico de unos 44.000 pacientes ya ha alcanzado la meta para ello: que se registrasen 170 contagios. De ellos, 162 infecciones se han dado en el grupo de personas que recibišź un placebo (agua con sales) y ocho en el que recibišź las dos dosis de la vacuna, lo que supone una eficacia del 95%. Esta eficacia aplica a todas las edades, sexos y razas de los participantes en el ensayo, realizado en gran parte en Estados Unidos. La efectividad en las personas mayores de 65 a?os es de un 94%. Los datos tambišŠn sugieren que la vacuna previene los casos graves de covid, pues de los 10 registrados, solo uno era del grupo vacunado, segšČn la compa?šȘa.
Con estos datos la empresa ha anunciado que va a solicitar Ą°en dšȘasĄ± el permiso de aprobacišźn de emergencia para esta vacuna a la agencia del medicamento de EE UU, la FDA, y que haršą lo mismo con otras agencias, como la europea. Este tipo de aprobacišźn es temporal y permite emplear un fšąrmaco o una vacuna antes de que hayan terminado los ensayos clšȘnicos, ya que el estudio de Pfizer tiene previsto continuar hasta 2022, sobre todo para entender cušąnto dura el efecto de la vacuna.
La vacuna podršȘa contar con la aprobacišźn de las autoridades de EE UU y de la Unišźn Europea en diciembre, segšČn ha explicado a Reuters Ugur Sahin, director ejecutivo de BioNTech. El responsable de la empresa alemana ha a?adido que intentan tener una nueva formulacišźn de su vacuna que no necesite conservarse en fršȘo ĄȘla actual necesita 70 grados bajo ceroĄȘ para la segunda mitad de 2021.
El anuncio de la compa?šȘa llega solo dos dšȘas despušŠs de que una de sus principales competidoras, Moderna, anunciase una eficacia de su vacuna del 94,5%, lo que superaba la inicialmente citada por Pfizer, del 90%. Esos datos se basaban en un nšČmero de infectados que no permitšȘan demostrar eficacia con plena validez estadšȘstica, algo que los 170 alcanzados ahora sšȘ permite. Una vez mšąs, el anuncio se ha hecho a travšŠs de un comunicado de prensa y no va acompa?ado de un estudio cientšȘfico en profundidad y revisado por expertos independientes. En los šČltimos meses, este tipo de anuncios han permitido a las empresas involucradas en el desarrollo de vacunas y fšąrmacos contra el covid aumentar de forma extraordinaria su capitalizacišźn en bolsa.
El comunicado informa de que la vacuna, desarrollada en colaboracišźn con la alemana BioNTech, ha sido bien tolerada por los participantes. Los šČnicos efectos adversos graves registrados han sido la fatiga, en el 3,8% de los casos, y el dolor de cabeza, en el 2%.
Pfizer ha dicho que este a?o podršą fabricar vacunas para 25 millones de personas y en 2021 para unos 650 millones. En la fabricacišźn participaršąn plantas de Pfizer en EE UU asšȘ como las de BioNTech en Alemania, ha dicho la compa?šȘa. Espa?a espera recibir vacunas para 10 millones de personas a principios de 2021, lo que permitiršȘa cubrir a buena parte de todos los mayores de 65 a?os y al personal sanitario.
Pfizer asegura que ha desarrollado contenedores para poder enviar la vacuna a la temperatura requerida de unos 70 grados bajo cero a Ą°todo el mundoĄ±. Estos contenedores contienen hielo seco que puede conservar la vacuna durante 15 dšȘas y ese plazo se puede ampliar rellenando la carga de hielo seco, ha explicado la empresa. En esto Moderna le lleva ventaja, pues su vacuna puede conservarse durante un mes en un frigoršȘfico convencional.
Ą°Estos datos son mšąs completos que los ofrecidos la semana pasada y se alcanzan las cifras para dar validez estadšȘstica a los resultados segšČn exigieron las agencias reguladoras como la FDA", se?ala Marcos Lšźpez, presidente de la Sociedad Espa?ola de InmunologšȘa. Ą°Con todas las cautelas, pues el ensayo clšȘnico ašČn no ha terminado y ašČn no se han publicado todos los datos cientšȘficos, la vacuna parece evitar los casos graves de covid. De todas formas queda una gran pregunta; ?cušąnto dura la inmunidad inducida por la vacuna? Esto no lo sabremos hasta que vayan saliendo mšąs datos intermedios del ensayo clšȘnico, que no tiene previsto acabar hasta diciembre de 2022Ą±, resalta.
Ą°Estos datos son prometedores, pero siguen siendo solo titulares; no tenemos los matices para ver el verdadero potencial de estas vacunasĄ±, opina Isabel Sola, viršźloga del CSIC. Ą°Seguimos necesitando los datos completos para confirmar que esta alta eficacia aplica a los casos mšąs severos. Dicen que la vacuna es segura, pero parece que ašČn no han terminado los dos meses despušŠs de la segunda dosis, que es el tiempo que exige la FDAĄ±, explica. Posiblemente por esto la compa?šȘa ha dicho que solicitaršą la aprobacišźn Ą°en dšȘasĄ±: tiene que esperar a que al menos la mitad de los vacunados lleven dos meses tras la šČltima dosis. Ą°Tampoco aclaran si la vacuna seršȘa eficaz tambišŠn en personas vulnerables menores de 65. Tampoco sabemos bien la clase de inmunidad que da (esterilizante o no) y, por supuesto, la duracišźn de la inmunidad.Ą±, a?ade Sola.
Las autoridades europeas ya han llegado a acuerdos preliminares para comprar mšąs de 1.200 millones de dosis de diferentes vacunas experimentales, como la desarrollada por la Universidad de Oxford y la farmacšŠutica britšąnica AstraZeneca, la del tšąndem BioNTech-Pfizer, la de la biotecnolšźgica alemana Curevac, la de la estadounidense Johnson & Johnson y la creada por la multinacional francesa Sanofi y la britšąnica GSK. Hay mšąs de 200 vacunas experimentales diferentes contra la covid, segšČn las cifras de la Organizacišźn Mundial de la Salud, y medio centenar ya se estšąn probando en humanos. De ellas, 11 candidatas estšąn en la recta final, con ensayos en decenas de miles de voluntarios.
Puedes seguir a MATERIA en Facebook, Twitter, Instagram o suscribirte aqušȘ a nuestra Newsletter.
Tu suscripcišźn se estšą usando en otro dispositivo
?Quieres a?adir otro usuario a tu suscripcišźn?
Si continšČas leyendo en este dispositivo, no se podršą leer en el otro.
FlechaTu suscripcišźn se estšą usando en otro dispositivo y solo puedes acceder a EL PA?S desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripcišźn a la modalidad Premium, asšȘ podršąs a?adir otro usuario. Cada uno accederšą con su propia cuenta de email, lo que os permitiršą personalizar vuestra experiencia en EL PA?S.
?Tienes una suscripcišźn de empresa? Accede aqušȘ para contratar mšąs cuentas.
En el caso de no saber quišŠn estšą usando tu cuenta, te recomendamos cambiar tu contrase?a aqušȘ.
Si decides continuar compartiendo tu cuenta, este mensaje se mostraršą en tu dispositivo y en el de la otra persona que estšą usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aqušȘ los tšŠrminos y condiciones de la suscripcišźn digital.
Sobre la firma