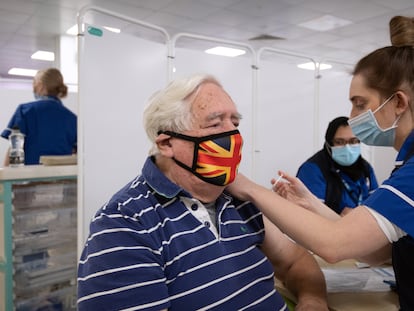
í░Esperar mĘós pruebas con miles de muertes no es precauciĘ«n, es tomar riesgosí▒
Kent Woods, que fue director de las agencias reguladoras de medicamentos en el Reino Unido y en la UE, critica la decisiʫn de no aplicar la vacuna de AstraZeneca a mayores de 55 a?os


Kent Woods (Yorkshire, Reino Unido, 72 a?os) fue director ejecutivo de la agencia reguladora de medicamentos en su paʬs (MHRA, por sus siglas en inglĘŽs) y de la europea (EMA) entre 2011 y 2015. Esta Ę▓ltima ha autorizado la vacuna de AstraZeneca para cualquier persona mayor de 18 a?os, pero un nĘ▓mero creciente de paʬses europeos estĘó poniendo el lʬmite en 65 o menos. Espa?a pone la barrera en los 55 a?os. Woods no entiende esta medida, que, considera, í░cuesta vidasí▒.
Pregunta. ?Por quʎ la EMA no incluyʫ un lʬmite de edad en su recomendaciʫn para la vacuna de AstraZeneca?
Respuesta. Aunque el nĘ▓mero de infecciones por covid-19 fue demasiado bajo en el ensayo de fase 3 para confirmar por separado que la vacuna es eficaz en este grupo de edad, la buena respuesta de anticuerpos sugiere que la vacuna serĘó protectora tanto en pacientes mayores como en mĘós jĘ«venes. La pregunta clave que debemos hacernos es la siguiente: ?Tenemos alguna razĘ«n para creer que la vacuna deja de ser eficaz despuĘŽs de cierta edad? La respuesta es claramente no. Esta ha sido la conclusiĘ«n a la que llegaron el comitĘŽ cientʬfico de la EMA y tambiĘŽn los evaluadores y el comitĘŽ de expertos de la MHRA a finales de diciembre.
P. Ha apuntado que hay intereses polʬticos en los paʬses que estĘón limitando esta vacuna a personas menores de 65 a?os (o 55 en algunos casos, como el de Espa?a) ?CuĘóles cree que son?
R. Los paʬses en los que los polʬticos han tomado esta posiciĘ«n, en particular Francia y Alemania, tienen representantes expertos en el comitĘŽ de productos para consumo humano de la EMA que no aplicaron esta restricciĘ«n de edad al acordar la posiciĘ«n. Realmente no entiendo por quĘŽ la posiciĘ«n polʬtica deberʬa ser diferente de la opiniĘ«n cientʬfica en el mismo paʬs. Al restringir el rango de edad de esta manera, estos paʬses no protegen a las mismas personas que estĘón en mayor riesgo de enfermedad grave y muerte por covid-19. í░Esperar mĘós pruebasí▒ puede parecer una precauciĘ«n, pero con miles de muertes diarias que ocurren en la UE (principalmente entre los ancianos) no es precauciĘ«n, es asumir riesgos. Al igual que el pedido tardʬo de vacunas y la lenta toma de decisiones reglamentarias, sugiere que los responsables polʬticos de la UE no han mostrado un sentido de urgencia suficiente durante la pandemia. Es difʬcil ver a quĘŽ interĘŽs polʬtico responderʬa esto; en cambio, me parece que surge de que la ComisiĘ«n dio prioridad a la í░armonizaciĘ«ní▒ y, como resultado, al tiempo que lleva llegar a un consenso.
P. ?Por quʎ cree que los comitʎs cientʬficos de estos paʬses recomiendan este lʬmite de edad?
R. Parece haber una falla de comunicaciĘ«n en esos paʬses entre los expertos en la evaluaciĘ«n de ensayos clʬnicos y aquellos que estĘón asesorando a sus Gobiernos en polʬticas de salud pĘ▓blica. En Alemania, por ejemplo, el Instituto Robert Koch tiene el liderazgo en el asesoramiento de salud pĘ▓blica, pero la agencia reguladora de medicamentos biolĘ«gicos como las vacunas es el Instituto Paul Ehrlich.
P. LlegĘ« a decir que los paʬses que deciden asʬ estĘón arriesgando la vida de su poblaciĘ«n.
R. Nadie ha planteado preocupaciones de seguridad sobre la vacuna Oxford-AstraZeneca. Las preocupaciones expresadas sobre su eficacia surgen de la renuencia a extrapolar los resultados en pacientes mĘós jĘ«venes a pacientes mayores. Aceptamos sin lugar a dudas que una vacuna que fue eficaz en sujetos del Reino Unido y Brasil funcionarĘó en ciudadanos de la UE (aunque ninguno de estos Ę▓ltimos se incluyĘ« en el ensayo); no hay ninguna razĘ«n por la que no deberʬa hacerlo. Siguiendo la misma lĘ«gica, ?hay alguna razĘ«n por la que la vacuna no deberʬa funcionar en los mayores de 65 a?os (donde se sabe que se da la respuesta de anticuerpos) cuando funciona en los menores de 65 a?os? Este falso razonamiento da como resultado que el grupo de edad mĘós vulnerable se vea privado de una vacuna que ya escasea en la UE. Como alguien perteneciente a ese rango de edad, me hubiera encantado recibir cualquiera de las dos, la de Pfizer-BioNTech o la de Oxford la semana pasada cuando asistʬ al centro de vacunaciĘ«n.
P. ?CuĘól es el precio que estamos pagando por este enfoque conservador?
R. RestringirĘó aĘ▓n mĘós la disponibilidad dentro de la UE de una vacuna eficaz en el mismo grupo de edad en el que se producen la mayorʬa de las muertes. AdemĘós, las opiniones encontradas de los lʬderes polʬticos sobre este tema solo aumentarĘón la confusiĘ«n y la renuencia a aceptar la vacunaciĘ«n entre la poblaciĘ«n, que en Francia, por ejemplo, ya tiene un alto nivel de incredulidad de las vacunas, que no se basa en evidencias.
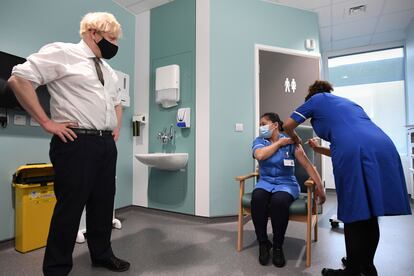
P. ?Existe un riesgo real al recomendar esta vacuna en los ancianos?
R. Nuestra experiencia en el Reino Unido, donde la vacunaciĘ«n avanza muy rĘópidamente con las vacunas de Pfizer y Oxford-AstraZeneca, es que los efectos secundarios observados han sido poco comunes, leves y totalmente en lʬnea con lo que cabrʬa esperar. No existe ningĘ▓n problema de seguridad conocido que justifique la restricciĘ«n de edad.
P. ?No cree que el mensaje de confianza podrʬa romperse si la vacuna de AstraZeneca finalmente no demuestra su eficacia en las personas mayores?
R. Si ese fuera el caso, pero por las razones que ya he dado, este es un resultado hipotĘŽtico. Lo que no es hipotĘŽtico, pero lamentablemente muy real, es la continua alta tasa de mortalidad por covid, particularmente entre los mayores de 65 a?os. El mayor peligro para la confianza del pĘ▓blico en las vacunas son los mensajes contradictorios que provienen de los polʬticos y de los cientʬficos.
P. ?Cree que la EMA estĘó siendo lo suficientemente Ęógil para aprobar las vacunas? Europa estĘó muy por detrĘós del Reino Unido y Estados Unidos.
R. Las decisiones de la EMA se retrasan por la necesidad de coordinar una opiniĘ«n cientʬfica en 27 Estados miembros. En este caso, habrʬa sido legalmente posible (pero polʬticamente inaceptable) basarse en la evaluaciĘ«n de la MHRA mediante un proceso de reconocimiento mutuo; el Reino Unido todavʬa estaba dentro de la UE en ese momento y la evaluaciĘ«n se habʬa llevado a cabo segĘ▓n los mismos estĘóndares de la UE. En el caso de la pandemia de gripe porcina de 2009, la MHRA liderĘ« la evaluaciĘ«n cientʬfica de las vacunas y esto fue aceptado por el comitĘŽ cientʬfico de la EMA. Por tanto, parece que existen factores tanto de procedimiento como polʬticos dentro de la ComisiĘ«n que han impedido que la EMA llegue a una conclusiĘ«n mĘós rĘópida.
P. En Espa?a estamos vacunando a todos los trabajadores sanitarios antes que a las personas mayores de 80 a?os. ?Tiene sentido?
R. En el Reino Unido, estamos dando la mĘóxima prioridad a las personas mayores de 80 a?os, pero los trabajadores de la salud y el personal de las residencias tambiĘŽn estĘón en la fila para recibir la vacuna antes que los menores de 65 a?os sanos. Las razones para dar a los trabajadores de la salud una vacunaciĘ«n temprana son poderosas: protegerlos de la exposiciĘ«n ocupacional; reducir los problemas de personal por ausencias por enfermedad; y reducir el riesgo de que el personal infectado presintomĘótico o no sintomĘótico infecte a los pacientes. Por tanto, no criticarʬa el enfoque espa?ol y probablemente no sea muy diferente del enfoque del Reino Unido en la prĘóctica.
P. ?Cree que el 70% o mĘós de la poblaciĘ«n del Reino Unido se vacunarĘó en verano? ?Y en Europa?
R. El Reino Unido estĘó actualmente en camino de vacunar a los mayores de 65 a?os, los trabajadores de salud mĘŽdicamente vulnerables y de primera lʬnea para el 15 de febrero. En esos grupos prioritarios (edad y condiciones de salud preexistentes) se encuentran entre el 85% y el 90% de las enfermedades graves y las muertes. Luego, se ofrecerĘó la vacuna al resto de la poblaciĘ«n adulta y es realista pensar que habremos cubierto al menos el 70% de toda la poblaciĘ«n adulta en junio o antes.
En la UE, el ritmo de vacunaciĘ«n hasta ahora ha sido mucho mĘós lento. Deberʬa acelerarse cuando la capacidad de fabricaciĘ«n de la vacuna Pfizer-BioNTech aumente en BĘŽlgica en las prĘ«ximas semanas y meses, y cuando se hayan resuelto los problemas de fabricaciĘ«n de la vacuna Oxford-AstraZeneca en la UE (en una escala de tiempo similar). Supongo que serĘó oto?o antes de que se logre una cobertura del 70% o mĘós en la mayorʬa de los paʬses de la UE, y tendrĘón diferentes sistemas para priorizar las vacunas.
Informaciʫn sobre el coronavirus
- Aquʬ puede seguir la Ę▓ltima hora sobre la evoluciĘ«n de la pandemia
- Buscador de restricciones: ?QuĘŽ puedo hacer en mi municipio?
- Asʬ evoluciona la curva del coronavirus en el mundo
Tu suscripciĘ«n se estĘó usando en otro dispositivo
?Quieres a?adir otro usuario a tu suscripciʫn?
Si continĘ▓as leyendo en este dispositivo, no se podrĘó leer en el otro.
FlechaTu suscripciĘ«n se estĘó usando en otro dispositivo y solo puedes acceder a EL PA?S desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripciĘ«n a la modalidad Premium, asʬ podrĘós a?adir otro usuario. Cada uno accederĘó con su propia cuenta de email, lo que os permitirĘó personalizar vuestra experiencia en EL PA?S.
En el caso de no saber quiĘŽn estĘó usando tu cuenta, te recomendamos cambiar tu contrase?a aquʬ.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrarĘó en tu dispositivo y en el de la otra persona que estĘó usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquʬ los tĘŽrminos y condiciones de la suscripciĘ«n digital.
Sobre la firma