Rebeli¿«n cient¿¬fica para que Europa apruebe el controvertido medicamento contra el alzh¿Ğimer
El nuevo anticuerpo monoclonal lecanemab solo beneficiar¿¬a al 5% de pacientes, seg¿▓n la Sociedad Espa?ola de Neurolog¿¬a, que aboga por aprobarlo

El primer f¿órmaco que ha mostrado alg¿▓n efecto contra el alzh¿Ğimer en varias d¿Ğcadas í¬el lecanemabí¬ est¿ó dividiendo a la comunidad cient¿¬fica y m¿Ğdica. Estados Unidos, China, Jap¿«n, Israel, Corea del Sur o Emiratos ?rabes ya han aprobado el uso de este anticuerpo monoclonal. Reino Unido le acaba de dar el visto bueno, pero su sistema p¿▓blico no lo suministrar¿ó, porque considera que sus efectos son demasiado modestos para su coste, de unos 24.000 euros al a?o por paciente. A contracorriente, la Agencia Europea del Medicamento (EMA) lo rechaz¿« en julio al considerar que sus beneficios í¬reduce un 27% el avance de la enfermedadí¬ no compensan los riesgos í¬hemorragias cerebrales y muerte de dos pacientesí¬.
El alzh¿Ğimer es la principal causa de demencia, y afecta a unos 50 millones de personas en el mundo. El envejecimiento de la poblaci¿«n amenaza con que estas cifras se multipliquen antes de mediados de siglo. Las asociaciones de pacientes han recibido la llegada de este medicamento con enorme esperanza, pero lo cierto es que la inmensa mayor¿¬a no podr¿ón beneficiarse de ¿Ğl, pues funciona solo en casos muy tempranos, antes de que la dolencia est¿Ğ avanzada. El donanemab, un segundo anticuerpo similar que reduce un 35% el avance del alzh¿Ğimer, tambi¿Ğn ha sido aprobado en Estados Unidos, pero sigue en evaluaci¿«n en Europa.
En un movimiento poco habitual, cuatro prestigiosos investigadores internacionales que llevan d¿Ğcadas estudiando esta enfermedad han enviado una carta abierta a EL PA?S para pedir que Europa reconsidere su decisi¿«n y apruebe esta clase de f¿órmacos. La decisi¿«n de la EMA í░niega el acceso a los pacientes y sus m¿Ğdicos a un tratamiento que puede cambiarles la vidaí▒, escriben Bart de Strooper, cofundador del Instituto de Investigaci¿«n de Demencia de Reino Unido, Henrik Zetterberg, de la Universidad de Gotemburgo (Suecia), Christian Haass, de M¿▓nich (Alemania), y John Hardy, del University College (Reino Unido).
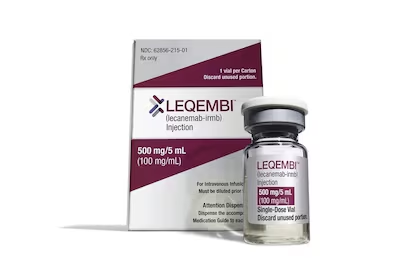
Los investigadores destacan la paradoja de que el lecanemab naci¿« en Europa, cuando en los a?os noventa el sueco Lars Lannfelt fund¿« una compa?¿¬a para desarrollar un anticuerpo monoclonal contra la prote¿¬na beta-amiloide, que se acumula en el cerebro de los pacientes. Posteriormente, la compa?¿¬a de Lannfelt fue adquirida por la japonesa Eisai, que finalmente ha desarrollado el medicamento junto a la estadounidense Biogen con el nombre comercial de Leqembi.
El no de Europa í░estrangulaí▒ la investigaci¿«n en este campo dentro de la Uni¿«n Europea, que queda posicionada í░como un seguidor, en lugar de un l¿¬derí▒, a?aden los firmantes.
Esta situaci¿«n í░se debe al fatalismo que existe respecto a la demenciaí▒, a?ade De Strooper por correo electr¿«nico. í░Un medicamento con la eficacia y los efectos secundarios de lecanemab ser¿¬a aceptado en otros campos de la medicina donde, como en este caso, no hay alternativa disponibleí▒. Hace unas semanas, Hardy alert¿« de que en Europa habr¿ó tratamientos de alzh¿Ğimer distintos para ricos, los que puedan viajar a Estados Unidos u otro pa¿¬s, y el resto de la poblaci¿«n.
La presi¿«n de los fabricantes por conseguir que se apruebe su producto es enorme. Biogen fue la principal impulsora de un anticuerpo monoclonal anterior, aducanumab. La Agencia del Medicamento de Estados Unidos (FDA) lo aprob¿« en contra del criterio de varios de sus expertos, que dimitieron como protesta. El compuesto acab¿« en un fracaso comercial millonario.
Los conflictos de intereses est¿ón en el centro de la pol¿Ğmica. Al contrario que la FDA, la EMA veta de sus paneles a cient¿¬ficos que tienen relaciones comerciales con las farmac¿Ğuticas. Precisamente de eso se quejan De Strooper, Zetterberg y el resto de firmantes: no les han dejado participar en el proceso de evaluaci¿«n de lecanemab porque son consultores habituales de varias empresas, incluida Eisai. Ambos cient¿¬ficos detallan a EL PA?S que en esas asesor¿¬as ganan unos 300 euros la hora, y que se trata de colaboraciones puntuales que no condicionan su opini¿«n como í░l¿¬deresí▒ de la investigaci¿«n en alzh¿Ğimer. Los investigadores quieren que sean los pacientes quienes decidan si toman el f¿órmaco considerando los riesgos.
Con los datos publicados hasta ahora, no hay forma de saber si lecanemab tiene un efecto cognitivo apreciable. El 27% de reducci¿«n de avance de la enfermedad puede traducirse en cinco meses ganados a la dolencia en un periodo de a?o y medio, pero no se sabe si esos beneficios contin¿▓an si se toma el f¿órmaco durante m¿ós tiempo. Las dos compa?¿¬as de Leqembi acaban de presentar datos de seguimiento de pacientes durante tres a?os en el Congreso de la Asociaci¿«n Internacional de Alzh¿Ğimer, celebrado en Filadelfia. Los resultados, que a¿▓n no han sido revisados pro expertos independientes, muestran que la mejora cognitiva se mantiene si se contin¿▓a el tratamiento y que estar¿¬a ya justo en el umbral de la relevancia cl¿¬nica.
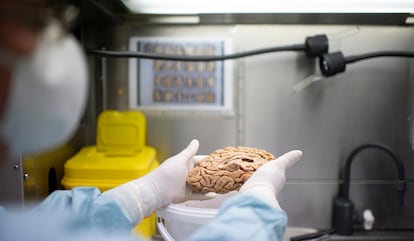
En el estudio original, que analiz¿« a unos 1.700 pacientes, unos 80 de ellos en Espa?a, los esc¿óneres cerebrales del 12% mostraron anomal¿¬as asociadas a la prote¿¬na amiloide que pueden producir inflamaci¿«n del cerebro y hemorragias. Dos pacientes murieron debido al uso del f¿órmaco. Las empresas dicen que los efectos secundarios se resuelven por s¿¬ solos en la mayor¿¬a de los casos y se concentran en los primeros meses de tratamiento. Hasta el momento no se han detectado m¿ós complicaciones, asegura un portavoz de Eisai.
En Estados Unidos, el lecanemab cuesta 26.500 d¿«lares al a?o, unos 24.000 euros. El pa¿¬s aprob¿« el f¿órmaco en enero de 2023, pero su llegada a los pacientes est¿ó siendo lenta por las dudas sobre su eficacia, su coste y los efectos secundarios, informa Reuters. El verano pasado, un estudio estim¿« que implantar Leqembi en Europa costar¿¬a 133.000 millones de euros, la mitad de todo el gasto farmac¿Ğutico de la UE. Pero esa cantidad podr¿¬a ser bastante menor debido a que muchas personas quedar¿¬an excluidas por contraindicaciones, como tomar anticoagulantes o tener el perfil gen¿Ğtico APOE4.
Estos nuevos f¿órmacos requieren un test gen¿Ğtico, una punci¿«n lumbar para determinar la cantidad de amiloide en el cerebro y varios esc¿óneres para descartar efectos secundarios. Adem¿ós, habr¿¬a que darlos de forma preventiva durante el resto de la vida. La dosis actual son dos inyecciones intravenosas que hay que poner en el hospital. La gran esperanza es que avance el diagn¿«stico temprano, sobre todo con an¿ólisis de sangre de prote¿¬na tau, que a¿▓n no son habituales en muchos hospitales.
Raquel S¿ónchez del Valle, coordinadora del grupo de conducta y demencias de la Sociedad Espa?ola de Neurolog¿¬a, reconoce que en el seno de su organizaci¿«n hay opiniones encontradas sobre el nuevo f¿órmaco. La neur¿«loga del Hospital Cl¿¬nic de Barcelona dice que en varias sociedades cient¿¬ficas europeas hay í░preocupaci¿«n porque los pacientes no puedan acceder a estos f¿órmacosí▒. El usuario de lecanemab ser¿¬a una persona que a¿▓n tiene independencia para vivir por s¿¬ mismo, pero empieza a tener faltas leves de memoria, como olvidar citas o repetir frases varias veces, explica. Seg¿▓n la SEN, el lecanemab estar¿¬a indicado solo para el 5% de los 800.000 enfermos de alzh¿Ğimer que hay en Espa?a. A pesar de ello, esta sociedad aboga por aprobar el lecanemab y que haya un seguimiento oficial de todos los pacientes. í░Los pa¿¬ses como Estados Unidos van a tener estos datos, y a nosotros en Europa nos gustar¿¬a tenerlos tambi¿Ğní▒.
Juan Fortea es neur¿«logo del Hospital Sant Pau de Barcelona, uno de los 12 que participan en el ensayo cl¿¬nico de Lecanemab en Espa?a. El m¿Ğdico destaca que este f¿órmaco no es una cura, y que í░nadie deber¿¬a fiarse de ninguna historia de ¿Ğxito personalí▒. í░A este f¿órmaco no le podemos pedir milagros, como la resurrecci¿«n de las neuronas que ya se han muerto cuando la enfermedad est¿ó avanzada. Lo que s¿¬ logra es que la ca¿¬da sea m¿ós lentaí▒, explica. Aunque a¿▓n í░es una inc¿«gnitaí▒ si los beneficios mostrados por el ensayo de 18 meses se acumulan en el tiempo, Fortea í░ni entiende ni comparte la decisi¿«n de la EMAí▒, porque í░no est¿ó justificadaí▒. El neur¿«logo cree que este tipo de f¿órmacos traen í░una nueva era en el tratamiento del alzh¿Ğimerí▒. í░Europa no puede ir contra el mundo. Con estos f¿órmacos el coste del tratamiento y los cuidados va a crecer mucho, pero es lo mismo que ya hemos visto en oncolog¿¬aí▒, opina.
Miguel Medina, director cient¿¬fico adjunto del Centro de Investigaci¿«n Biom¿Ğdica en Red sobre Enfermedades Neurodegenerativas, es m¿ós esc¿Ğptico. í░La EMA siempre es m¿ós conservadora que la FDA, y en este caso la situaci¿«n se ha complicado por la historia del aducanumab [el fracasado f¿órmaco anterior] y los conflictos de inter¿Ğs, que es un asunto de por s¿¬ muy delicado, porque hay investigadores muy atados a las empresasí▒, advierte. í░Es cierto que los m¿Ğdicos y los investigadores cl¿¬nicos son m¿ós partidarios de aprobar el f¿órmaco, sobre todo por tener algo que ofrecer a los pacientes. Pero tambi¿Ğn hay efectos adversos que afectar¿¬an a personas de unos 65 a?os a las que a¿▓n les pueden quedar unos buenos a?os de vida. Puede que haya que aceptar a expertos que colaboran con farmac¿Ğuticas, aunque yo prefiero ser estricto con los conflictos de inter¿Ğs. Las agencias tienen que ser muy cuidadosasí▒, a?ade.
Toda la presi¿«n cae ahora sobre la EMA. Su Comit¿Ğ de Productos M¿Ğdicos para Uso Humano tiene un presidente, un miembro por cada pa¿¬s de la Uni¿«n Europea y hasta cinco expertos adicionales propuestos por cada pa¿¬s. El organismo no recomend¿« aprobar lecanemab en julio. La farmac¿Ğutica Eisai recurri¿« la decisi¿«n, y se espera que el comit¿Ğ vuelva a reunirse para tomar una resoluci¿«n final antes de final de a?o.
Tu suscripci¿«n se est¿ó usando en otro dispositivo
?Quieres a?adir otro usuario a tu suscripci¿«n?
Si contin¿▓as leyendo en este dispositivo, no se podr¿ó leer en el otro.
FlechaTu suscripci¿«n se est¿ó usando en otro dispositivo y solo puedes acceder a EL PA?S desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripci¿«n a la modalidad Premium, as¿¬ podr¿ós a?adir otro usuario. Cada uno acceder¿ó con su propia cuenta de email, lo que os permitir¿ó personalizar vuestra experiencia en EL PA?S.
?Tienes una suscripci¿«n de empresa? Accede aqu¿¬ para contratar m¿ós cuentas.
En el caso de no saber qui¿Ğn est¿ó usando tu cuenta, te recomendamos cambiar tu contrase?a aqu¿¬.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrar¿ó en tu dispositivo y en el de la otra persona que est¿ó usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aqu¿¬ los t¿Ğrminos y condiciones de la suscripci¿«n digital.
Sobre la firma































































